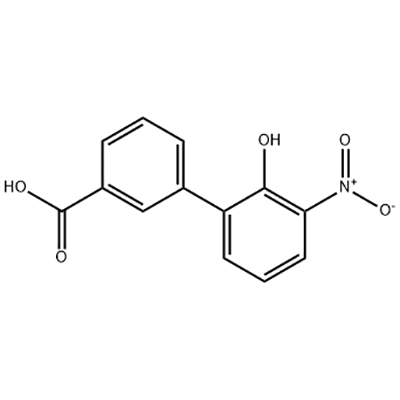
2′-hydroxy-3′-nitro-3-biphenylcarboxylic acid
2′-hydroxy-3′-nitro-3-biphenylcarboxylic acid
Ang 2'-hydroxy-3'-nitro-3-biphenylcarboxylic acid ay ginagamit bilang intermediate ng Eltrombopag .
Ang Eltrombopag, na binuo ng GlaxoSmithKline (GSK) sa UK at kalaunan ay pinagsama-samang binuo kasama ang Novartis sa Switzerland, ang una at tanging naaprubahang maliit na molekula na hindi peptide TPO receptor agonist sa mundo.Ang Eltrombopag ay inaprubahan ng US FDA noong 2008 para sa paggamot ng idiopathic thrombocytopenic purpura (ITP), at noong 2014 para sa paggamot ng malubhang aplastic anemia (AA).Ito rin ang unang gamot na inaprubahan ng US FDA para sa paggamot sa AA sa nakalipas na 30 taon.
Noong Disyembre 2012, inaprubahan ng US FDA ang Eltrombopag para sa paggamot ng thrombocytopenia sa mga pasyente na may talamak na hepatitis C (CHC), upang ang mga pasyente ng hepatitis C na may mahinang pagbabala dahil sa mababang bilang ng platelet ay maaaring magsimula at mapanatili ang interferon based na standard na therapy para sa mga sakit sa atay.Noong february3,2014, inihayag ng GlaxoSmithKline na ipinagkaloob ng FDA ang pambihirang paggamot na kwalipikasyon ng gamot ng Eltrombopag para sa paggamot ng hemopenia sa mga pasyenteng may malubhang chemicalbook aplastic anemia (SAA) na hindi ganap na tumugon sa immunotherapy.Noong Agosto 24, 2015, inaprubahan ng US FDA ang Eltrombopag para sa paggamot ng thrombocytopenia sa mga nasa hustong gulang at bata na 1 taong gulang pataas na may talamak na immune thrombocytopenia (ITP) na walang sapat na tugon sa corticosteroids, immunoglobulins o splenectomy.Noong Enero4,2018, naaprubahan ang Eltrombopag na mailista sa China para sa paggamot ng pangunahing immune thrombocytopenia (ITP).


![Casp ungin Acetate;Caspofungin acetate;Cancidas;Caspofungin acetate [USAN:BAN:JAN];](http://cdn.globalso.com/jindunchem-med/fbe17385-300x300.jpg)


![2-butyl-5-nitro-3-benzofuranyl)[4-[3-(dibutylaMino)propoxy]phenyl]](http://cdn.globalso.com/jindunchem-med/922e79ba.jpg)
